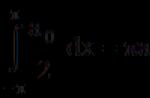План лекции:
1. Понятие ковалентной связи.
2. Электроотрицательность.
3. Полярная и неполярная ковалентная связь.
Ковалентная связь образуется за счёт общих электронных пар, возникающих в оболочках связываемых атомов.
Она может быть образована атомами одного итого же элемента и тогда она неполярная; например, такая ковалентная связь существует в молекулах одноэлементных газов H 2 , O 2 , N 2 , Cl 2 и др.
Ковалентная связь может быть образована атомами разных элементов, сходных по химическому характеру, и тогда она полярная; например, такая ковалентная связь существует в молекулах H 2 O, NF 3 , CO 2 .
Неоходимо ввести понятие электроотрицательность.
Электроотрицательность – это способность атомов химического элемента оттягивать к себе общие электронные пары, участвующие в образовании химической связи.
ряд электроотрицательностей
Элементы с большей электроотрицательностью будут оттягивать общие электроны от элементов с меньшей электроотрицательностью.
Для наглядного изображения ковалентной связи в химических формулах используются точки (каждая точка отвечает валентному электрону, а также черта отвечает общей электронной паре).
Пример. Связи в молекуле Cl 2 можно изобразить так:
Такие записи формул равнозначны. Ковалентные связи обладают пространственной направленностью. В результате ковалентного связывания атомов образуются либо молекулы, либо атомные кристаллические решётки со строго определенным геометрическим расположением атомов. Каждому веществу соответствует своя структура.
С позиции теории Бора образование ковалентной связи объясняется тенденцией атомов преобразовывать свой внешний слой в октет (полное заполнение до 8 электронов).Оба атома представляют для образования ковалентной связи по одному неспаренному электрону, и оба электрона становятся общими.
Пример. Образование молекулы хлора.

Точками обозначены электроны. При расстановке следует соблюдать правило:электроны ставятся в определённой последовательности-слева, сверху, справа,снизу по одному, затем добавляют по одному, неспаренные электроны и принимают участие в образовании связи.
Новая электронная пара, возникшая из двух неспаренных электронов, становится общей для двух атомов хлора. Существует несколько способов образования ковалентных связей за счёт перекрывания электронных облаков.
|
|
|
|
|
σ – связь значительно прочнее π-связи, причём π-связь может быть только с σ-связью, За счёт этой связи образуются двойные и тройные кратные связи.
Полярные ковалентные связи образуются между атомами с разной электроотрицательностью.
За счёт смещения электронов от водорода к хлору атом хлора заряжается частично отрицательно, водорода-частично положительно.
Полярная и неполярная ковалентная связь
Если двухатомная молекула состоит из атомов одного элемента, то электронное облако распределяется в пространстве симметрично относительно ядер атомов. Такая ковалентная связь называется неполярной. Если ковалентная связь образуется между атомами различных элементов, то общее электронное облако смещено в сторону одного из атомов. В этом случае ковалентная связь является полярной. Для оценки способности атома притягивать к себе общую электронную пару используют величину электроотрицательности.
В результате образования полярной ковалентной связи более электроотрицательный атом приобретает частичный отрицательный заряд, а атом с меньшей электроотри-цательностью – частичный положительный заряд. Эти заряды принято называть эффективными зарядами атомов в молекуле. Они могут иметь дробную величину. Например, в молекуле HСl эффективный заряд равен 0,17e (где е – заряд электронаЗаряд электрона равен 1,602 . 10 -19 Кл.):
Система из двух равных по величине, но противоположных по знаку зарядов, расположенных на определенном расстоянии друг от друга, называется электрическим диполем. Очевидно, что полярная молекула является микроскопическим диполем. Хотя суммарный заряд диполя равен нулю, в окружающем его пространстве существует электрическое поле, напряженность которого пропорциональна дипольному моменту m:
В системе СИ дипольный момент измеряется в Кл×м, но обычно для полярных молекул в качестве единицы измерения используется дебай (единица названа в честь П. Дебая):
1 D = 3,33×10 –30 Кл×м
Дипольный момент служит количественной мерой полярности молекулы. Для многоатомных молекул дипольный момент представляет собой векторную сумму дипольных моментов химических связей. Поэтому, если молекула симметрична, то она может быть неполярной, даже если каждая из ее связей обладает значительным дипольным моментом. Например, в плоской молекуле BF 3 или в линейной молекуле BeCl 2 сумма дипольных моментов связей равна нулю:
Аналогично, нулевой дипольный момент имеют тетраэдрические молекулы CH 4 и CBr 4 . Однако, нарушение симметрии, например в молекуле BF 2 Cl, обусловливает дипольный момент, отличный от нуля.
Предельным случаем ковалентной полярной связи является ионная связь. Она образуется атомами, электроотрицательности которых значительно различаются. При образовании ионной связи происходит почти полный переход связующей электронной пары к одному из атомов, и образуются положительный и отрицательный ионы, удерживаемые вблизи друг друга электростатическими силами. Поскольку электростатическое притяжение к данному иону действует на любые ионы противоположного знака независимо от направления, ионная связь, в отличие от ковалентной, характеризуется ненаправленностью и ненасыщаемостью . Молекулы с наиболее выраженной ионной связью образуются из атомов типичных металлов и типичных неметаллов (NaCl, CsF и т.п.), т.е. когда различие в электроотрицательности атомов велико.
В которой один из атомов отдавал электрон и становился катионом , а другой атом принимал электрон и становился анионом .
Характерные свойства ковалентной связи - направленность, насыщаемость, полярность, поляризуемость - определяют химические и физические свойства соединений.
Направленность связи обусловлена молекулярным строением вещества и геометрической формы их молекулы. Углы между двумя связями называют валентными.
Насыщаемость - способность атомов образовывать ограниченное число ковалентных связей. Количество связей, образуемых атомом, ограничено числом его внешних атомных орбиталей.
Полярность связи обусловлена неравномерным распределением электронной плотности вследствие различий в электроотрицательностях атомов. По этому признаку ковалентные связи подразделяются на неполярные и полярные (неполярные - двухатомная молекула состоит из одинаковых атомов (H 2 , Cl 2 , N 2) и электронные облака каждого атома распределяются симметрично относительно этих атомов; полярные - двухатомная молекула состоит из атомов разных химических элементов, и общее электронное облако смещается в сторону одного из атомов, образуя тем самым асимметрию распределения электрического заряда в молекуле, порождая дипольный момент молекулы).
Поляризуемость связи выражается в смещении электронов связи под влиянием внешнего электрического поля, в том числе и другой реагирующей частицы. Поляризуемость определяется подвижностью электронов . Полярность и поляризуемость ковалентных связей определяет реакционную способность молекул по отношению к полярным реагентам.
Однако, дважды лауреат Нобелевской премии Л. Полинг указывал, что «в некоторых молекулах имеются ковалентные связи, обусловленные одним или тремя электронами вместо общей пары» . Одноэлектронная химическая связь реализуется в молекулярном ионе водорода H 2 + .
Молекулярный ион водорода H 2 + содержит два протона и один электрон. Единственный электрон молекулярной системы компенсирует электростатическое отталкивание двух протонов и удерживает их на расстоянии 1,06 Å (длина химической связи H 2 +). Центр электронной плотности электронного облака молекулярной системы равноудалён от обоих протонов на боровский радиус α 0 =0,53 А и является центром симметрии молекулярного иона водорода H 2 + .
Энциклопедичный YouTube
-
1 / 5
Ковалентная связь образуется парой электронов, поделённой между двумя атомами, причём эти электроны должны занимать две устойчивые орбитали, по одной от каждого атома .
A· + ·В → А: В
В результате обобществления электроны образуют заполненный энергетический уровень. Связь образуется, если их суммарная энергия на этом уровне будет меньше, чем в первоначальном состоянии (а разница в энергии будет ни чем иным, как энергией связи).
Согласно теории молекулярных орбиталей, перекрывание двух атомных орбиталей приводит в простейшем случае к образованию двух молекулярных орбиталей (МО): связывающей МО и антисвязывающей (разрыхляющей) МО . Обобществлённые электроны располагаются на более низкой по энергии связывающей МО.
Образование связи при рекомбинации атомов
Однако, механизм межатомного взаимодействия долгое время оставался неизвестным. Лишь в 1930 г. Ф. Лондон ввёл понятие дисперсионное притяжение - взаимодействие между мгновенным и наведённым (индуцированными) диполями. В настоящее время силы притяжения, обусловленные взаимодействием между флуктуирующими электрическими диполями атомов и молекул носят название «Лондоновские силы ».
Энергия такого взаимодействия прямо пропорциональна квадрату электронной поляризуемости α и обратно пропорциональна расстоянию между двумя атомами или молекулами в шестой степени .
Образование связи по донорно-акцепторному механизму
Кроме изложенного в предыдущем разделе гомогенного механизма образования ковалентной связи, существует гетерогенный механизм - взаимодействие разноименно заряженных ионов - протона H + и отрицательного иона водорода H - , называемого гидрид-ионом :
H + + H - → H 2
При сближении ионов двухэлектронное облако (электронная пара) гидрид-иона притягивается к протону и в конечном счёте становится общим для обоих ядер водорода, то есть превращается в связывающую электронную пару. Частица, поставляющая электронную пару, называется донором, а частица, принимающая эту электронную пару, называется акцептором. Такой механизм образования ковалентной связи называется донорно-акцепторным .
H + + H 2 O → H 3 O +
Протон атакует неподелённую электронную пару молекулы воды и образует устойчивый катион, существующий в водных растворах кислот .
Аналогично происходит присоединение протона к молекуле аммиака с образованием комплексного катиона аммония :
NH 3 + H + → NH 4 +
Таким путём (по донорно-акцепторному механизму образования ковалентной связи) получают большой класс ониевых соединений , в состав которого входят аммониевые , оксониевые, фосфониевые, сульфониевые и другие соединения .
В качестве донора электронной пары может выступать молекула водорода, которая при контакте с протоном приводит к образованию молекулярного иона водорода H 3 + :
H 2 + H + → H 3 +
Связывающая электронная пара молекулярного иона водорода H 3 + принадлежит одновременно трём протонам.
Виды ковалентной связи
Существуют три вида ковалентной химической связи, отличающихся механизмом образования:
1. Простая ковалентная связь . Для её образования каждый из атомов предоставляет по одному неспаренному электрону. При образовании простой ковалентной связи формальные заряды атомов остаются неизменными.
- Если атомы, образующие простую ковалентную связь, одинаковы, то истинные заряды атомов в молекуле также одинаковы, поскольку атомы, образующие связь, в равной степени владеют обобществлённой электронной парой. Такая связь называется неполярной ковалентной связью . Такую связь имеют простые вещества , например: 2 , 2 , 2 . Но не только неметаллы одного типа могут образовывать ковалентную неполярную связь. Ковалентную неполярную связь могут образовывать также элементы-неметаллы, электроотрицательность которых имеет равное значение, например, в молекуле PH 3 связь является ковалентной неполярной, так как ЭО водорода равна ЭО фосфора.
- Если атомы различны, то степень владения обобществлённой парой электронов определяется различием в электроотрицательностях атомов. Атом с большей электроотрицательностью сильнее притягивает к себе пару электронов связи, и его истинный заряд становится отрицательным. Атом с меньшей электроотрицательностью приобретает, соответственно, такой же по величине положительный заряд. Если соединение образуется между двумя различными неметаллами , то такое соединение называется ковалентной полярной связью .
В молекуле этилена С 2 Н 4 имеется двойная связь СН 2 =СН 2 , его электронная формула: Н:С::С:Н. Ядра всех атомов этилена расположены в одной плоскости. Три электронных облака каждого атома углерода образуют три ковалентные связи с другими атомами в одной плоскости (с углами между ними примерно 120°). Облако четвёртого валентного электрона атома углерода располагается над и под плоскостью молекулы. Такие электронные облака обоих атомов углерода, частично перекрываясь выше и ниже плоскости молекулы, образуют вторую связь между атомами углерода. Первую, более прочную ковалентную связь между атомами углерода называют σ-связью; вторую, менее прочную ковалентную связь называют π {\displaystyle \pi } -связью.
В линейной молекуле ацетилена
Н-С≡С-Н (Н: С::: С: Н)
имеются σ-связи между атомами углерода и водорода, одна σ-связь между двумя атомами углерода и две π {\displaystyle \pi } -связи между этими же атомами углерода. Две π {\displaystyle \pi } -связи расположены над сферой действия σ-связи в двух взаимно перпендикулярных плоскостях.
Все шесть атомов углерода циклической молекулы бензола С 6 H 6 лежат в одной плоскости. Между атомами углерода в плоскости кольца действуют σ-связи; такие же связи имеются у каждого атома углерода с атомами водорода. На осуществление этих связей атомы углерода затрачивают по три электрона. Облака четвёртых валентных электронов атомов углерода, имеющих форму восьмерок, расположены перпендикулярно к плоскости молекулы бензола. Каждое такое облако перекрывается одинаково с электронными облаками соседних атомов углерода. В молекуле бензола образуются не три отдельные π {\displaystyle \pi } -связи, а единая π {\displaystyle \pi } диэлектрики или полупроводники . Типичными примерами атомных кристаллов (атомы в которых соединены между собой ковалентными (атомными) связями) могут служить
Благодаря которой образуются молекулы неорганических и органических веществ. Химическая связь появляется при взаимодействии электрических полей, которые создаются ядрами и электронами атомов. Следовательно, образование ковалентной химической связи связано с электрической природой.
Что такое связь
Под этим термином подразумевают результат действия двух либо более атомов, которые приводят к формированию прочной многоатомной системы. Основные виды химической связи образуются при уменьшении энергии реагирующих атомов. В процессе формирования связи атомы стараются завершить свою электронную оболочку.
Виды связи
В химии выделяют несколько видов связи: ионной, ковалентной, металлической. Ковалентная химическая связь имеет две разновидности: полярная, неполярная.
Каков механизм ее создания? Ковалентная неполярная химическая связь образуется между атомами одинаковых неметаллов, имеющих одну электроотрицательность. При этом образуются общие электронные пары.

Неполярная связь
Среди примеров молекул, у которых ковалентная химическая связь неполярного вида, можно назвать галогены, водород, азот, кислород.
Впервые эта связь была обнаружена в 1916 году американским химиком Льюисом. Сначала им была выдвинута гипотеза, а подтверждена она была только после экспериментального подтверждения.
Ковалентная химическая связь связана с электроотрицательностью. У неметаллов она имеет высокое значение. В ходе химического взаимодействия атомов не всегда возможен перенос электронов от одного атома к другому, в результате осуществляется их объединение. Между атомами появляется подлинная ковалентная химическая связь. 8 класс обычной школьной программы предполагает детальное рассмотрение нескольких видов связи.
Вещества, имеющие данный вид связи, при нормальных условиях - жидкости, газы, а также твердые вещества, имеющие невысокую температуру плавления.

Типы ковалентной связи
Подробнее остановимся на данном вопросе. Какие выделяют типы химической связи? Ковалентная связь существует в обменном, донорно-акцепторном вариантах.
Первый тип характеризуется отдачей каждым атомом одного неспаренного электрона на образование общей электронной связи.
Электроны, объединяемые в общую связь, должны обладать противоположными спинами. В качестве примера подобного вида ковалентной связи можно рассмотреть водород. При сближении его атомов наблюдается проникновение их электронных облаков друг в друга, именуемое в науке перекрыванием электронных облаков. В результате увеличивается электронная плотность между ядрами, а энергия системы понижается.
При минимальном расстоянии ядра водорода отталкиваются, в итоге образуется некое оптимальное расстояние.
В случае донорно-акцепторного типа ковалентной связи у одной частицы есть электроны, ее называют донором. Вторая частица имеет свободную ячейку, в которой будет размещаться пара электронов.

Полярные молекулы
Как образуются ковалентные полярные химические связи? Они возникают в тех ситуациях, когда у связываемых атомов неметаллов различная электроотрицательность. В подобных случаях обобществленные электроны размещаются ближе к тому атому, у которого значение электроотрицательности выше. В качестве примера ковалентной полярной связи могут рассматриваться связи, которые возникают в молекуле бромоводорода. Здесь общественные электроны, которые отвечают за формирование ковалентной связи, ближе находятся к брому, чем к водороду. Причина подобного явления в том, что у брома электроотрицательность выше, чем у водорода.

Способы определения ковалентной связи
Как определить ковалентные полярные химические связи? Для этого необходимо знать состав молекул. Если в ней присутствуют атомы разных элементов, в молекуле существует ковалентная полярная связь. В неполярных молекулах присутствуют атомы одного химического элемента. Среди тех заданий, которые предлагаются в рамках школьного курса химии, есть и такие, которые предполагают выявление вида связи. Задания подобного типа включены в задания итоговой аттестации по химии в 9 классе, а также в тесты единого государственного экзамена по химии в 11 классе.
Ионная связь
Чем отличается ковалентная и ионная химическая связь? Если ковалентная связь характерна для неметаллов, то ионная связь образуется между атомами, имеющими существенные отличия по электроотрицательности. К примеру, это характерно для соединений элементов первой и второй групп главных подгрупп ПС (щелочных и щелочноземельных металлов) и элементов 6 и 7 групп главных подгрупп таблицы Менделеева (халькогенов и галогенов).
Она формируется в результате электростатического притяжения ионов, обладающих противоположными зарядами.

Особенности ионной связи
Так как силовые поля противоположно заряженных ионов распределяются равномерно во всех направлениях, каждый из них способен притягивать к себе противоположные по знаку частицы. Это и характеризует ненаправленность ионной связи.
Взаимодействие двух ионов, обладающих противоположными знаками, не предполагает полной взаимной компенсации индивидуальных силовых полей. Это способствует сохранению способности притягивать по остальным направлениям ионы, следовательно, наблюдается ненасыщенность ионной связи.
В ионном соединении у каждого иона есть возможность притягивать к себе некое число других, обладающих противоположных знаком, чтобы сформировать кристаллическую решетку ионного характера. В таком кристалле не существует молекул. Каждый ион окружается в веществе неким конкретным числом ионов иного знака.
Металлическая связь
Данный вид химической связи обладает определенными индивидуальными особенностями. Металлы имеют избыточное количество валентных орбиталей при недостатке электронов.
При сближении отдельных атомов происходит перекрывание их валентных орбиталей, что способствует свободному перемещению электронов из одной орбитали в другую, осуществляя между всеми атомами металла связь. Эти свободные электроны и являются основным признаком металлической связи. Она не обладает насыщенностью и направленностью, поскольку валентные электроны распределяются по кристаллу равномерно. Присутствие в металлах свободных электронов объясняет их некоторые физические свойства: металлический блеск, пластичность, ковкость, теплопроводность, непрозрачность.
Разновидность ковалентной связи
Она образуется между атомом водорода и элементом, который имеет высокую электроотрицательность. Существуют внутри- и межмолекулярные водородные связи. Эта разновидность ковалентной связи является самой непрочной, она появляется благодаря действию электростатических сил. У атома водорода небольшой радиус, и при смещении либо отдаче этого одного электрона водород становится положительным ионом, действующим на атом с большой электроотрицательностью.
Среди характерных свойств ковалентной связи выделяют: насыщаемость, направленность, поляризуемость, полярность. Каждый из этих показателей имеет определенное значение для образуемого соединения. К примеру, направленность обуславливается геометрической формой молекулы.
Данные по энергии ионизации (ЭИ), ПЭИ и составу стабильных молекул - их настоящие значения и сравнения - как свободных атомов, так и атомов, связанных в молекулы, позволяют нам понять как атомы образуют молекулы посредством механизма ковалентной связи.
КОВАЛЕНТНАЯ СВЯЗЬ - (от латинского «со» совместно и «vales» имеющий силу) (гомеополярная связь), химическая связь между двумя атомами, возникающая при обобществлении электронов, принадлежавших этим атомам. Ковалентной связью соединены атомы в молекулах простых газов. Связь, при которой имеется одна общая пара электронов, называется одинарной; существуют также двойные и тройные связи.
Рассмотрим несколько примеров, чтобы увидеть, как мы можем использовать наши правила для определения количества ковалентных химических связей, которые может образовать атом, если мы знаем количество электронов на внешней оболочке данного атома и заряд его ядра. Заряд ядра и количество электронов на внешней оболочке определяются экспериментальным путем и включены в таблицу элементов.
Расчет возможного числа ковалентных связей
Для примера, подсчитаем количество ковалентных связей, которые могут образовать натрий (Na), алюминий (Al), фосфор (P), и хлор (Cl) . Натрий (Na) и алюминий (Al) имеют, соответственно 1 и 3 электрона на внешней оболочке, и, по первому правилу (для механизма образования ковалентной связи используется один электрон на внешней оболочке), они могут образовать:натрий (Na) - 1 и алюминий (Al) - 3 ковалентных связи. После образования связей количество электронов на внешних оболочках натрия (Na) и алюминия (Al) равно, соответственно, 2 и 6; т.е., менее максимального количества (8) для этих атомов. Фосфор (P) и хлор (Cl) имеют, соответственно, 5 и 7 электронов на внешней оболочке и, согласно второй из вышеназванных закономерностей, они могли бы образовать 5 и 7 ковалентных связей. В соответствии с четвертой закономерностью образование ковалентной связи, число электронов на внешней оболочке этих атомов увеличивается на 1. Согласно шестой закономерности, когда образуется ковалентная связь, число электронов на внешней оболочке связываемых атомов не может быть более 8. То есть, фосфор (P) может образовать только 3 связи (8-5 = 3), в то время как хлор (Cl) может образовать только одну (8-7 = 1).
Пример: на основании анализа мы обнаружили, что некое вещество состоит из атомов натрия (Na) и хлора (Cl) . Зная закономерности механизма образования ковалентных связей, мы можем сказать, что натрий (Na ) может образовать только 1 ковалентную связь. Таким образом, мы можем предположить, что каждый атом натрия (Na) связан с атомом хлора (Cl) посредством ковалентной связи в этом веществе, и что это вещество состоит из молекул атома NaCl . Формула строения для этой молекулы: Na - Cl. Здесь тире (-) означает ковалентную связь. Электронную формулу этой молекулы можно показать следующим образом:
. .
Na: Cl:
. .
В соответствии с электронной формулой, на внешней оболочке атома натрия (Na) в NaCl имеется 2 электрона, а на внешней оболочке атома хлора (Cl) находится 8 электронов. В данной формуле электроны (точки) между атомами натрия (Na) и хлора (Cl) являются связующими электронами. Поскольку ПЭИ у хлора (Cl) равен 13 эВ, а у натрия (Na) он равен 5,14 эВ, связующая пара электронов находится гораздо ближе к атому Cl , чем к атому Na . Если энергии ионизации атомов, образующих молекулу сильно различаются, то образовавшаяся связь будет полярной ковалентной связью.Рассмотрим другой случай. На основании анализа мы обнаружили, что некое вещество состоит из атомов алюминия (Al) и атомов хлора (Cl) . У алюминия (Al) имеется 3 электрона на внешней оболочке; таким образом, он может образовать 3 ковалентные химические связи, в то время хлор (Cl) , как и в предыдущем случае, может образовать только 1 связь. Это вещество представлено как AlCl 3 , а его электронную формулу можно проиллюстрировать следующим образом:
Рисунок 3.1. Электронная формула AlCl 3
чья формула строения:
Cl - Al - Cl
ClЭта электронная формула показывает, что у AlCl 3 на внешней оболочке атомов хлора (Cl ) имеется 8 электронов, в то время, как на внешней оболочке атома алюминия (Al) их 6. По механизму образования ковалентной связи, оба связующих электрона (по одному от каждого атома) поступают на внешние оболочки связываемых атомов.
Кратные ковалентные связи
Атомы, имеющие более одного электрона на внешней оболочке, могут образовывать не одну, а несколько ковалентных связей между собой. Такие связи называются многократными (чаще кратными ) связями. Примерами таких связей служат связи молекул азота (N = N ) и кислорода (O = O ).
Связь, образующаяся при объединении одинарных атомов называется гомоатомной ковалентной связью,е сли атомы разные, то связь называется гетероатомнной ковалентной связью [греческие префексы "гомо" и "гетеро" соответственно означают одинаковые и разные].
Представим, как в действительности выглядит молекула со спаренными атомами. Самая простая молекула со спаренными атомами - это молекула водорода.
Ковалентная химическая связь возникает между атомами с близкими или равными значениями электроотрицательностей. Предположим, что хлор и водород стремятся отнять электроны и принять структуру ближайшего благородного газа, значит ни один из них не отдаст электрон другому. Каким же способом они все таки соединяются? Все просто – они поделятся друг с другом, образуется общая электронная пара.

Теперь рассмотрим отличительные черты ковалентной связи.
В отличие от ионных соединений, молекулы ковалентных соединений удерживаются вместе за счет «межмолекулярных сил», которые намного слабее химических связей. В связи с этим, ковалентной связи характерна насыщаемость – образование ограниченного числа связей.
Известно, что атомные орбитали ориентированы в пространстве определенным образом, поэтому при образовании связи, перекрывание электронных облаков происходит в определенном направлении. Т.е. реализуется такое свойство ковалентной связи как направленность.
Если ковалентная связь в молекуле образована одинаковыми атомами или атомами с равной электроотрицательностью, то такая связь не имеет полярности, т.е электронная плотность распределяется симметрично. Называется она неполярной ковалентной связью ( H 2 , Cl 2 , O 2 ). Связи могут быть как одинарными, так и двойными, тройными.
Если электроотрицательности атомов различаются, то при их соединении электронная плотность распределяется между атомами неравномерно и образуется ковалентная полярная связь (HCl, H 2 O, CO), кратность которой также может быть различной. При образовании данного типа связи, более электроотрицательный атом приобретает частичный отрицательный заряд, а атом с меньшей электроотрицательностью – частичный положительный заряд (δ- и δ+). Образуется электрический диполь, в котором заряды, противоположные по знаку, расположены на неком расстоянии друг от друга. В качестве меры полярности связи используют дипольный момент:

Полярность соединения тем более выражена, чем больше дипольный момент. Молекулы будут иметь неполярный характер, если дипольный момент равен нулю.
В связи с вышеперечисленными особенностями, можно заключить, что ковалентные соединения летучи, имеют низкие температуры плавления и кипения. Электрический ток не может проходить через эти соединения, следовательно, они плохие проводники и хорошие изоляторы. При подводе тепла, многие соединения с ковалентной связью, загораются. В большей части это углеводороды, а также оксиды, сульфиды, галогениды неметаллов и переходных металлов.
Категории ,