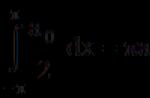Реакция нейтрализации (например, серной кислоты) в водоеме за счет бикарбонатов кальция протекает по формуле Са(НС03)24-Н2304=Са304+2Н20+2С02.[ ...]
Нейтрализация известняком не всегда эффективна, так как в присутствии серной кислоты гипс, образующийся на поверхности частиц известняка, тормозит дальнейший ход реакции нейтрализации.[ ...]
Реакция нейтрализации - это химическая реакция между веществами, имеющими свойства кислоты и основания, которая приводит к потере характерных свойств обоих соединений. Наиболее типичная реакция нейтрализации в водных растворах происходит между гидратированными ионами водорода и ионами гидроксида, содержащимися соответственно в сильных кислотах и основаниях: Н+ + 0Н =Н20. В результате концентрация каждого из этих ионов становится равной той, которая свойственна самой воде (около 10 7), т. е. активная реакция водной среды приближается к рН=7.[ ...]
Реакция взаимодействия основания с кислотой, в результате которой получается соль и вода, является реакцией нейтрализации.[ ...]
Нейтрализация фильтрацией заключается в том, что сточную жидкость пропускают через слой фильтрующего материала. При прохождении жидкости через такой фильтр реакция нейтрализации должна полностью заканчиваться. В качестве фильтрующего материала для нейтрализации кислот применяют известняк, мрамор и доломит. Этот способ имеет ряд преимуществ: он более прост и дешев, эффективен при неравномерной концентрации кислот в сточных водах.[ ...]
Реакцию нейтрализации кислот можно проводить также и с помощью других реагентов типа оснований. Расход этих веществ для нейтрализации 1 г различных кислот (стехиометрично) приведен в табл. 6.[ ...]
Реакция нейтрализации и вычисление по этой реакции количества неизвестного вещества имеет очень широкое применение в агрохимических лабораториях. Подобного рода вычисления возможны по всем химическим правильно составленным уравнениям.[ ...]
Реакция нейтрализации протекает очень быстро, и при дальнейшем смешивании вся масса сточных вод приобретает одинаковое значение pH в течение нескольких минут.[ ...]
Для нейтрализации вод первого типа могут быть использованы любые из указанных выше реагентов. При нейтрализации вод второго типа соли не только выпадают в осадок, но при больших концентрациях могут отлагаться на поверхности нейтрализующего материала и тормозить ход реакции. Нейтрализация вод третьего типа возможна только растворами щелочей.[ ...]
При реакции нейтрализации серной кислоты с известью или мелом на 98 частей кислоты получаются 172 части двуводного гипса СаЗОд. 2Н20.[ ...]
Способ нейтрализации фильтрованием состоит в том, что кислую сточную воду после предварительного осветления пропускают через слой нейтрализующего материала с такой скоростью, чтобы за время соприкосновения воды с материалом реакция нейтрализации закончилась.[ ...]
В камере реакции не только нейтрализуется свободная кислота, но и заканчивается кристаллизация солей кальция и хлопье-образование гидроокисей металлов, что приводит к окончательной стабилизации pH. С этой точки зрения установка датчика после камер реакции является наиболее рациональной. Однако следует иметь в виду, что устройство устойчивой системы регулирования при помощи промышленных приборов крайне осложняется, если время транспортного запаздывания превышает 10- 15 мин. Исходя из этих соображений, нередко приходится отказываться от расположения датчика регулирующего прибора после камеры реакции, рассчитанной на более чем десятиминутное пребывание воды. В этом случае датчик регулирующего прибора можно устанавливать на выходе из смесителя или где-либо по пути движения воды между смесителем и камерой реакции (или отстойником)-там, где реакция нейтрализации прошла с наибольшей полнотой. В эксплуатационных условиях такое место легко найти путем испытания проб, взятых последовательно по пути движения воды, смешанной с реагентом. Там, где во взятой пробе величина pH остается неизменной после тщательного перемешивания, и замеряется значение регулирующего параметра.[ ...]
Реагенты для нейтрализации кислых сточных вод выбирают в зависимости от вида кислот и их концентрации. Кроме того, учитывают, образуется ли в процессе реакции нейтрализации осадок. Для нейтрализации минеральных кислот применяют любой щелочной реагент, но чаще всего следующие: известь в виде пушонки или известкового молока, а также карбонаты кальция или магния в виде суспензии.[ ...]
Метод основан на реакции нейтрализации салициловой кислоты щелочью. Конец реакции фиксируется потенциометром.[ ...]
Выбор реагента для нейтрализации кислых сточных вод зависит от вида кислот и их концентрации, а также от растворимости солей, образующихся в результате химической реакции. Для нейтрализации минеральных кислот применяют любой щелочной реагент, но чаще всего известь в виде пушонки или известкового молока и карбонаты кальция или магния в виде суспензии. Эти реагенты сравнительно дешевы и общедоступны, но имеют ряд недостатков: при этом обязательно устройство усреднителей перед нейтрализационной установкой, затруднительно регулирование дозы реагента по pH нейтрализованной воды, сложно реагентное хозяйство. Скорость реакции между раствором кислоты и твердыми частицами суспензии относительно невелика и зависит от размеров частиц и растворимости образующегося в результате реакции нейтрализации соединения. Поэтому окончательная активная реакция в жидкой фазе устанавливается не сразу, а по истечении некоторого времени (10-15 мин). Сказанное выше относится к сточным водам, содержащим сильные кислоты (Н2504, Н2503), кальциевые соли которых труднорастворимы в воде.[ ...]
Чтобы контролировать реакцию нейтрализации, надо знать, какое количество кислоты или щелочи следует добавить в раствор для получения необходимого значения pH. Для решений этой проблемы может быть использован метод эмпирической оценки стехиометрических коэффициентов, которая осуществляется с помощью титрования.[ ...]
Как видим, знаменитую реакцию аннигиляции е+ +е = 2Ь можно рассматривать, причем логично и обоснованно, как реакцию нейтрализации - вывод, по-моему, не только интересный, но и изящный.[ ...]
Для полного окончания реакции нейтрализации и флокуляции взвеси сточные воды, протекая через резервуар, перемешиваются сжатым воздухом (с целью окисления Ре2+ до Ре3+) или механическим путем. В флоку-лятор (или нейтрализующий резервуар) добавляют соответствующее количество флокулирующих средств, способствующих образованию плотных агломератов из легко осаждаемой взвеси. Флокулятор должен быть в три-шесть раз больше резервуара нейтрализатора.[ ...]
Из представленных выше реакций нейтрализации можно подсчитать, что в стехиометрических условиях расход СаО на 1 г соответствующих соединений будет следующим: H2SO4 - 0,56 г; FeS04 - 0,37 г; НС1-0,77 г; FeCl2 - 0,44 г; HN03 - 0,44 г; Fe(N03h - 0,31 г; Н3РО4 -0,86 г.[ ...]
Важно подчеркнуть, что в реакциях нейтрализации ОН-, образующихся при растворении карбонатов и силикатов, участвуют не только угольная кислота, но и органические кислоты (особенно фульво- и гуминовые), являющиеся агентом интенсивного разложения пород. Сильная диссоциация многих органических кислот приводит к увеличению в воде концентраций Н. Константы диссоциации таких распространенных в природе соединений, как фульво- и гуминовые кислоты, приближаются к и-10-3-« 10"5. Это означает, что они могут снижать pH реальных подземных вод до 3 и менее. В связи с зтим такие органические кислоты интенсивно разлагают силикаты с разрушением их кристаллической решетки. Степень такого разложения тем больше, чем ниже минерализация подземных вод и чем более кислыми они являются.[ ...]
Пример 6. Вычислить продолжительность реакции нейтрализации кислых растворов известковой суспензией, если реакция проводится в периодическом реакторе идеального смещения (РИС-П) .[ ...]
Самую простую систему очистки на основе реакции нейтрализации можно представить в виде измельченного известняка, на который вылили раствор кислоты, а осадок собрали в отстойник.[ ...]
Анализ колебаний концентраций и механизм реакций нейтрализации кислотных железосодержащих сточных вод послужили основанием для выбора параметров регулирования этого процесса. Стало очевидным, что регулировать подачу нейтрализующего реагента только по одному показателю pH недостаточно. Необходим второй параметр, который мог бы реагировать на наличие в воде сернокислого железа и влиять на подачу реагента в соответствии с его текущими концентрациями.[ ...]
С целью обеспечения1 полноты и ускорения хода реакции нейтрализации и осаждения солей тяжелых металлов в камерах реакции производится непрерывное перемешивание сточных вод пропеллерными или лопастными мешалками с вертикальной осью вращения. Частота вращения мешалки принимается не менее 40 мин-1; при частоте вращения 150 мин-1 продолжительность контакта сточных вод, содержащих ионы тяжелых металлов может быть сокращена до 15 мин.[ ...]
Процессы химического улавливания примесей используют для нейтрализации наиболее крупномасштабных загрязнителей окружающей среды: оксидов азота, сернистого ангидрида, сероводорода, галогенов и др. Поскольку конкретные реакции нейтрализации каждого из этих веществ индивидуальны, удобнее имеющиеся способы очистки рассматривать применительно к перечисленным основным газовым загрязнителям.[ ...]
Как видим, все получается весьма строго и логично: в обоих случаях реакция нейтрализации сводится к со единению ионов лиония и лиата; в обеих реакциях получается в качестве продукта нейтрализации соль - хлористый калий.[ ...]
Цри защелачивании нефти можно не учитывать расход реагентов на сероводород, так как в первую очередь в реакцию вступает хлористый водород как более сильная кислота.[ ...]
Реактор можно рассматривать как изолированную систему (потери тепла в окружающую среду незначительные), а процессы нейтрализации, происходящие в нем, являются самопроизвольными и необратимыми. В реакторе будет выделяться в результате реакций нейтрализации около 2,5 Мкал/ч, что, очевидно, соответствует повышению свободной энергии активных веществ отходов при их образовании на промышленных предприятиях.[ ...]
Излюбленное критическое замечание по отношению к теории сольвосистем заключалось в том, что она не может описывать кислотно-основные реакции не в «своем растворителе».[ ...]
Для предупреждения коррозии канализационных очистных сооружений, нарушения биохимических процессов в биологических окислителях и водоисточниках, а также осаждения из сточных вся солей тяжелых металлов, кислые и щелочные воды подвергаются нейтрализации. Наиболее типичная реакция нейтрализации - это реакция между ионами водорода и гидроксила, приводящая к образованию малодиссоциированной воды; Н++ОЬГ = Н20. В результате реакции концентрация каяедого из этих ионов становится одинаковой (около 107), т.е. активная реакция водной среды приближается к pH = 7.[ ...]
Основной причиной образования осадков является взаимодействие сточных вод с пластовыми, когда происходит изменение среды растворов в направлении приближения к pH пластовой воды, т. е. к равновесным пластовым условиям, как правило, близким к нейтральным. Нейтрализация сопровождается гидролизом компонентов сбросных вод. В отдельных случаях за счет контакта с кислыми и щелочными средами может происходить частичное растворение пород, слагающих пласт с последующими, практически неконтролируемыми вторичными образованиями осадков в результате реакций нейтрализации. Кроме того, одной из причин образования осадков может быть введение со сточными водами компонентов, реагирующих с компонентами пластовой воды, в результате чего образуются осадки даже без изменения среды растворов.[ ...]
Электроды, используемые для титрования кислот и оснований, являются индикаторными по отношению к концентрации ионов водорода. Мы рассмотрим два типа электродов: сурьмяный и стеклянный, которые, на наш взгляд, могут с успехом применяться в санитарно-химическом анализе для реакции нейтрализации и определения pH растворов.[ ...]
Нельзя, однако, согласиться, будто вся азотная кислота, выделяемая нитрифицирующими бактериями при окислении азотистой кислоты в почве, будет нейтрализоваться только за счет разложения фосфоритной муки. Даже в некарбонатных почвах почвенный раствор содержит бикарбонат кальция, который станет прежде всего участвовать в реакции нейтрализации (как наиболее подвижный) азотной кислоты. Кроме того, во всякой почве находится значительное количество обменнопоглощенного кальция, легко вытесняемого в раствор водородными ионами азотной кислоты с образованием кальциевой селитры.[ ...]
В клееной бумаге с проклейкой гидрофобным клеем внутри-волоконная диффузия, как свидетельствуют эксперименты, может осуществляться примерно в 1000 раз быстрее, чем через капилляры, проникновению воды в которые препятствуют гидрофобные частицы проклеивающего вещества. Добавление в воду раствора щелочи облегчает диффузию влаги в толщу бумажного листа, так как щелочь способствует набуханию волокон и, следовательно, внутриволоконнбму проникновению влаги. Кроме того, щелочь вступает в реакцию нейтрализации со свободной смолой канифольного клея, вследствие чего создаются условия, способствующие межволоконному проникновению влаги. Именно поэтому добавление в воду щелочного раствора способствует также капиллярному поднятию влаги в полосках бумаги, вертикально подвешенных над поверхностью влаги и касающихся этой поверхности.[ ...]
При таком способе изготовления смесей их выпускают в гранулированном виде, что обеспечивает хорошую их рассеваемость и облегчает применение локальным способом при посеве и посадке растений (в рядки, лунки, борозды). Эти удобрения называются уже сложно-смешанными. Для приготовления их берут в желательной пропорции отвешенные количества простых или сложных порошковидных удобрений (простого или двойного суперфосфата, аммофоса или диаммофоса, аммиачной селитры или мочевины и хлористого калия) и основательно их перемешивают в особом бара-бане-грануляторе. При этом добавляют аммиак для нейтрализации свободной фосфорной кислоты суперфосфата. Реакция нейтрализации протекает с выделением тепла и разогреванием смеси, что способствует ее подсушиванию. Если в смесь не вводят аммофоса или диаммофоса, то ее обогащают жидкой фосфорной кислотой. Благодаря вращению барабана из перемешиваемых порошковидных удобрений образуются гранулы. Их охлаждают, просеивают и обрабатывают водоотталкивающими веществами (чтобы исключить отсыревание). Готовые смеси упаковывают в 5-слойные бумажные мешки или в мешки из полиэтилена. Для выпуска тукосмесей по этому принципу в СССР строится 12 больших заводов с автоматизацией процессов.[ ...]
Впрочем, отметив, что электрон в основных растворителях находится «в свободном состоянии», мы допустили некоторую неточность. Разумеется, такая ничтожная по размерам частица обладает электростатическим полем исключительно высокой напряженности, и поэтому она будет притягивать к себе полярные молекулы растворителя, то есть будет сольватирована. Сольвати-рованный электрон известен и в водных растворах, где он образуется, например, при облучении воды и водных растворов источниками радиоактивного излучения. Но если в воде сольватированный электрон существует весьма непродолжительное время (всегда «к его услугам» в воде имеется достаточно ионов Н30+, чтобы произошла реакция нейтрализации: Н30+ + £-> У2Н2 ■+ ’ + Н20), то в сильноосновных растворителях сольватированный электрон весьма устойчив. Так, растворы натрия в жидком аммиаке хранятся без каких-либо изменений физических и химических свойств в течение нескольких месяцев.[ ...]
Серная кислота из заводского хранилища поступает в емкость, откуда погружным насосом подается в напорный бак, а затем в барабанный реактор. В соответствии с ГОСТом в сульфате алюминия ограничивается содержание свободной серной кислоты и нерастворимого остатка. Выполнение этих требований при непрерывном процессе возможно при наличии автоматической дозировки реагентов - суспензии гидроксида алюминия и серной кислоты. Центробежный насос непрерывно подает суспензию в циркуляционное кольцо, в верхней части которого расположена отборная коробка. Из отборной коробки часть суспензии поступает в барабанный реактор непрерывного действия, а избыток сливается в репульпатор. За счет теплоты разбавления серной кислоты и реакции нейтрализации гидроксида алюминия кислотой температура в реакторе поддерживается в пределах 95-115 °С. Продолжительность пребывания реакционной массы в реакторе составляет 25-40 мин. Плотность реакционной массы 1500 кг/м3. Производительность аппарата составляет 10000 кг/ч при скорости вращения барабана 0,18 с-1. По выходе из реактора концентрированный раствор сульфата алюминия с 13,5 % АЬОз поступает в распыливающие форсунки гранулятора кипящего слоя.
Видов реакции нейтрализации. Сама реакция подразумевает под собой гашение очагов (микробов, кислот и токсинов).
Реакция нейтрализации в медицине
В реакция нейтрализации используется в микробиологии. Основано это на том, что некоторые соединения способны связать возбудители различных заболеваний, или их метаболизмы. В итоге микроорганизмы лишаются возможности использовать свои биологические свойства. Сюда же можно отнести реакции торможения вирусов.Нейтрализация токсинов происходит по подобному принципу. В качестве основного компонента используют различные антитоксины, которые блокируют действие токсинов, не давая проявить им свои свойства.
Реакция нейтрализации в неорганической химии
Реакции нейтрализации - одна из основ неорганической . Нейтрализация относится к типу реакции обмена. На выходе реакции получается соль и вода. Для реакции используют кислоты и основания. Реакции нейтрализации обратимые и необратимые.Необратимые реакции
Обратимость реакции зависит от степени диссоциации составляющих. Если используются два сильных соединения, то реакция нейтрализации не сможет вернуться до исходных веществ. Это можно увидеть, например, при реакции гидроксида калия с азотной кислотой:КОН + HNO3 – KNO3 + Н2O;
Реакция нейтрализации в конкретном случае переходит в реакцию гидролиза соли.
В ионном виде реакция выглядит так:
Н(+) + OН(-) > Н2O;
Отсюда можно сделать вывод, что при реакции сильной кислоты с сильным основанием обратимости быть не может.
Обратимые реакции
Если реакция происходит между слабым основанием и сильной кислотой, либо слабой кислотой и сильным основанием, либо между слабой кислотой и слабым основанием, то процесс этот обратим.Обратимость происходит в результате смещения вправо в системе равновесия. Обратимость реакции можно увидеть при использовании в качестве исходных веществ, например, или синильной кислоты, а также аммиака.
Слабая кислота и сильное основание:
HCN+KOH=KCN+H2O;
В ионном виде:
HCN+OH(-)=CN(-)+H2O.
Слабое основание и
Тема урока: «Реакция нейтрализации как пример реакции обмена»
Цель урока: формировать представление о реакции нейтрализации как частном случае реакции обмена.
Задачи:
Создать условия для развития представлений о реакции нейтрализации как частном случае реакции обмена;
Расширить знания учащихся о свойствах кислот и оснований;
Продолжить развитие умений составления уравнений химических реакций;
Воспитывать наблюдательность и внимание в ходе проведения демонстрационного эксперимента.
Тип урока : комбинированный
Оборудование и реактивы : соляная кислота, растворы гидроксида натрия, гидроксида меди (II), фенолфталеин, пробирки.
Ход урока
Организационный момент.
Ребята давайте продолжим наше путешествие по стране под название Химия. На прошлом уроке мы знакомились с городом под названием Основания и с его жителями. Основные жители данного города – это основания. Дайте определение понятию «основание». Ну а теперь давайте проверим, как вы справились с домашним заданием.
Проверка домашнего задания.
№ 7, 8.
Опрос и дальнейшая актуализация знаний.
Какие классы неорганических веществ вы знаете?
Дайте определение понятиям «оксиды», «кислоты», «соли».
С какими веществами реагирует вода?
Какие вещества образуются при реакции воды с основными и кислотными оксидами?
Как доказать, что в результате взаимодействия воды с кислотным оксидом образуется кислота?
Что такое индикаторы?
О каком индикаторе идёт речь?
От щелочи я жёлт, как в лихорадке,
Краснею от кислот, как от стыда.
И я ищу спасительную влагу,
Чтоб не смогла заесть меня среда.
(Метилоранж.)
Попасть в кислоту для него неудача,
Но он перетерпит без вздоха и плача.
Зато в щелочах у такого блондина
Начнётся не жизнь, а сплошная малина.
(Фенолфталеин.)
Какие ещё индикаторы вы знаете?
Дайте определение понятиям «кислотный оксид», «основный оксид».
На какие группы делятся основания?
В какой цвет окрашивается фенолфталеин, метилоранж, лакмус в растворе щелочи?
Изучение нового материала.
Вы уже знаете, что щелочи это растворимые основания, при работе с ними необходимо соблюдать особые правила безопасного поведения, так как они оказывают разъедающее действие на нашу кожу. Но их можно «обезвредить», добавив к ним раствор кислоты – нейтрализовать. И тема сегодняшнего урока: «Реакция нейтрализации как пример реакции обмена» (запись темы на доске и в тетради).
Цель сегодняшнего урока: формировать представление о реакции нейтрализации; научится записывать уравнения реакций нейтрализации.
Давайте вспомним, какие вы уже знаете типы химических реакций. Определите тип данных реакциях
Na 2 O + H 2 O = 2 NaOH
2H 2 O = 2H 2 + O 2
Zn + 2HCl =ZnCl 2 +H 2
Дайте определение данным типам реакций.
Так же вы уже знаете, что если к щелочи добавить фенолфталеин, то раствор станет малинового цвета. Но если к этому раствору добавить кислоту, окраска исчезает (дем. взаимодействия NaOH и HCl ). Это произошла реакция нейтрализации.
Запись уравнения на доске: NaOH + HCl = NaCl + H 2 O
В результате получается соль и вода.
Давайте все вместе попробуем дать определение реакции нейтрализации.
Реакция нейтрализации не относится ни к одному из известных до сих пор типов реакций. Это реакция обмена. Общая схема реакции обмена: AB +CD =AD + CB
То есть это реакция между сложными веществами, в ходе которых они обмениваются своими составными частями.
А кто знает, какая кислота находится у нас в желудке? Как вы думаете, почему при изжоге рекомендуется, если под рукой нет таблетки, выпить немного раствора соды?
Дело в том, что раствор соды тоже имеет щелочную среду и когда мы выпиваем этот раствор, происходит реакция нейтрализации. Раствор соды нейтрализует соляную кислоту, находящую в нашем желудке.
Как вы думаете, вступают ли в реакцию с кислотами нерастворимые основания? (Ответы учащихся). Дем. взаимодействия Cu(OH) 2 и HCl .
Запись уравнения на доске: Cu(OH) 2 + 2 HCl = CuCl 2 + 2 H 2 O .
Закрепление
Допишите следующие уравнения реакций:
а ) KOH+ H 2 SO 4 = …;
б ) Fe(OH) 2 + HCl =…;
в ) Ca(OH) 2 + H 2 SO 4 =…. .
Какие исходные вещества необходимо взять для получения следующих солей по реакции нейтрализации: Ca ( NO 3 ) 2 ; NaI ; BaSO 4.
Даны вещества: HCl ; H 2 SO 4 ; Fe ( OH ) 3 . Составьте уравнения всех возможных реакций нейтрализации между ними.
Физкультминутка: Учитель показывает вещества, а учащимся необходимо определить к какому классу веществ относится вещество и выполнять следующие действия: оксид – руки вверх, соль – встать, кислота – руки в стороны, основания – ничего не делать.
Обобщение
Закончите предложенную схему
Основные классы неорганических веществ
СО 2 ; Na 2 O ? ? ?
Н 2 SO 4 ; HCl NaOH;Ca(OH) 2 CaCl 2; Na 2 SO 4
2.Закончите нижеприведённые предложения:
Группа атомов ОН называется …..
Валентность этой группы постоянная и равна ….
Основания состоят из атомов …. и одной или нескольких …. .
К химическим свойствам оснований можно отнести их действие на … .При этом индикаторы приобретают окраску: лакмус - ….; фенолфталеин - ….; метилоранж - … .
Кроме того, основания вступают в реакцию с …. .
Эта реакция называется реакцией …
Продуктами этой реакции являются …. и …. .
Реакция обмена – это реакция между …. веществами, при которой они обмениваются своими … частями.
Реакция нейтрализации – это частный случай реакции … .
VII Рефлексия
Что на сегодняшнем уроке нового вы узнали? Достигли ли мы целей, поставленных на уроке?
Домашнее задание: § 33 № 6, подготовится к практической работе № 6
Дополнительная информация: Знаете ли вы, что женщины Древней Руси мыли волосы раствором еловой золы или золы подсолнечника? Раствор золы мылкий на ощупь и называется «щелок». Такой раствор имеет щелочную среду, как и вещества, которые мы изучаем. По-арабски зола – «аль-кали».
Историческое названия важнейших щелочей: гидроксид натрия – едкий натр, гидроксида калия – едкий кали. Щелочи используются для производства стекла и мыла.
Загадка:
В ней металл и кислород,
Да ещё плюс водород.
И такое сочетание
Называют -….. (основание)
Леонид Чуешков
Впереди всегда здесь «аш»,
А за ним что остаётся.
Она щиплется и жжётся.
И на первый взгляд проста,
А зовётся - … (кислота)
Леонид Чуешков
Cтраница 2
Реакции нейтрализации, в которых участвует слабая кислота или слабое основание, протекают не полностью, только до установления равновесия.
Реакции нейтрализации являются экзотермическими процессами (Н ОН-Н2О 57 3 кДж), следовательно, гидролиз солей эн-дотермичен.
Реакции нейтрализации являются экзотермическими процессами (Н ОН - Н2О 57 3 кДж), следовательно, гидролиз солей эндотермичен.
Реакция нейтрализации - это химическая реакция между веществом, имеющим свойства кислоты, и веществом, имеющим свойства основания, которая приводит к потере характерных свойств обоих соединений. Наиболее типичная реакция нейтрализации в водных растворах происходит между гидратированными ионами водорода и ионами гидро-ксила, содержащимися соответственно в сильных кислотах и основаниях: Н ОН-Н2О.
Реакция нейтрализации протекает не только в водных, но и в неводных растворах. Химическая природа неводного растворителя влияет на состояние ионов в растворе и на степень диссоциации. Одно и то же вещество может быть в одном растворителе солью, в другом кислотой, в третьем основанием.
Реакция нейтрализации сопровождается выделением теплоты; поэтому термометр Бекмана предварительно устанавливают таким образом, чтобы в начале опыта ртуть в капилляре термометра была в нижней части шкалы. После того как будет собран калориметр, определяют его постоянную (см. предыдущую работу), вставив в крышку калориметра пустую ампулу.
Реакции нейтрализации протекают с выделением тепла. Однако количество тепла, высвобождаемого при смешении разбавленных кислот и щелочей, трудно оценить на ощупь. Концентрированные же кислоты и основания ни в коем случае не следует смешивать друг с другом. Такая смесь становится настолько горячей, что начинает кипеть и сильно расплескиваться.
Реакции нейтрализации играют решающую роль при формовании, так как они предопределяют кинетику осаждения и структуру образующейся нити. Кроме того, в результате реакции нейтрализации ряд продуктов переходит в неустойчивую форму и разлагается.
Реакция нейтрализации щелочью нафтеновых кислот и фенолов имеет обратимый характер. Нафтенаты и феноляты в присутствии воды гидролизуются, образуя исходные продукты. Степень гидролиза зависит от условий процесса. Она увеличивается с повышением температуры и понижается с ростом концентрации раствора щелочи. Щелочную очистку целесообразно проводить при невысоких температурах, используя концентрированные растворы.
Реакции нейтрализации, протекающие в водных растворах, аналогичны реакциям, происходящим в неводных средах.
Реакция нейтрализации представляет собой ионообменную реакцию и проходит моментально. В отличие от нее реакция этерификации не является ионообменной и протекает медленнее. И реакция образования этилатов, и реакция этерификации обратимы, а следовательно, ограничены состоянием равновесия.
Нейтрализация – химическая реакция, происходящая между двумя составами, имеющими свойства кислоты и основания. В результате их взаимодействия происходит потеря свойств обоих веществ, что приводит к выделению соли и воды.
Сфера применения нейтрализации
Вычисления по этой реакции особенно часто используются:
- в агрохимических лабораториях;
- в химическом производстве;
- при обработке отходов.
Метод нейтрализации применяется в клинических лабораториях для определения буферной емкости плазмы крови, кислотности желудочного сока. Активно используется и в фармакологии, когда нужно провести количественный анализ неорганических и органических кислот. Проводить этот процесс можно по всем правильно составленным уравнениям.
Внешние проявления нейтрализации
Процесс нейтрализации кислоты можно наблюдать, если вначале к раствору добавить несколько капель индикатора, который позволит изменить окраску раствора. Когда к этой смеси добавляется щелочь, то окраска полностью исчезает. Но стоит учитывать, что индикаторы меняют свою окраску не строго в эквивалентной точке, а с отклонением. Поэтому даже при правильном выборе индикатора допускается погрешность. Если же он был выбран неправильно, то все результаты оказываются искаженными.
В условиях школьной программы для этого применяют лимонную кислоту и нашатырный спирт. В качестве примера можно рассмотреть процесс реакции между соляной кислотой и едким натром. В результате их взаимодействия образовывается известный всем раствор пищевой соли в воде. Также в качестве индикаторов могут выступать:
- метиловый оранжевый;
- лакмус;
- метиловый красный;
- фенолфталеин.
Необходимо отметить, что реакция, обратная нейтрализации, называется гидролизом. Его результатом является образование слабой кислоты или основания.
При выборе нейтрализующего вещества обязательно учитываются:
- промышленные свойства соединения;
- доступность;
- себестоимость.
Раньше в качестве нейтрализатора применяли окись магния. Сейчас она не пользуется популярностью, поскольку имеет высокую стоимость и вступает в реакцию достаточно медленно.
Виды реакции нейтрализации
В процессе взаимодействия сильного основания такой же сильной кислотой происходит смещение реакции в сторону образования воды. Вместе с тем этот процесс не доходит до конца, поскольку начинается гидролиз соли.
При нейтрализации слабой кислоты сильным основанием можно говорить об обратимой реакции. Как правило, в таких системах протекание реакции смещается в сторону образования соли, поскольку вода является более слабым электролитом, чем, например, синильная, уксусная кислота или аммиак.
Скорость процесса нейтрализации изменяется в зависимости от специфики используемых веществ. Например, при применении NaOH необходимая степень кислотности появляется практически сразу же. СаО приводит к возникновению нужной реакции только через 15-20 минут, а MgO – через 45 минут. При этом в последних двух случаях наиболее сильное понижение кислотности наблюдается в первые 5 минут после того как было внесено нейтрализующее вещество. Если скорость процесса не очень высокая, то еще больше его начинает тормозить вторичное окисление.
Выделение тепла в процессе нейтрализации
Часто это происходит под воздействием азотной кислоты. Чем выше ее количество, тем больше выделяется тепла. При получении поваренной соли воздействие тепла приводит к нежелательным последствиям, поскольку она начинает разлагаться с выделением хлора. Из-за выделения тепла можно говорить о том, что все реакции нейтрализации являются экзотермическими. Его выделение происходит из-за возникновения разницы между суммарной энергией ионов Н+ и ОН-, а также энергией образования молекул воды.